Lääkkeiden ja lääkinnällisten tuotteiden saatavuuden edistäminen

YK:n kestävän kehityksen tavoite 3:

3.4 Vähentää vuoteen 2030 mennessä kolmanneksella tarttumattomien tautien aiheuttamia ennenaikaisia kuolemia ennaltaehkäisyn ja hoidon avulla sekä edistää henkistä terveyttä ja hyvinvointia.
3.8 Saavuttaa yleiskattava terveydenhuolto, mukaan lukien turva taloudellisilta riskeiltä, pääsy laadukkaiden ja olennaisten terveydenhoitopalvelujen piiriin sekä turvalliset, tehokkaat, laadukkaat ja edulliset välttämättömät lääkkeet ja rokotukset kaikille.
Haasteet
Kroonisiin sairauksiin – kuten sydän ja verisuonitauteihin, syöpiin, diabetekseen ja hengityselinsairauksiin – liittyvä kuolleisuus on edelleen kansainvälisesti keskeinen terveyden indikaattori. Suomessa näitä sairauksia pidetään merkittävinä kansantauteina, ja oikea aikainen sekä tarkoituksenmukainen lääkehoito on olennainen osa oireiden hallintaa, sairauksien etenemisen hidastamista ja elämänlaadun parantamista.
Globaali toimintaympäristö aiheuttaa jatkuvasti haasteita lääkkeiden ja lääkinnällisten laitteiden saatavuudelle. Häiriöitä voi syntyä esimerkiksi maailmanpoliittisista jännitteistä, raaka aineiden saatavuusongelmista, tuotantoketjujen haavoittuvuuksista ja markkinakysynnän nopeista muutoksista. Useimmiten potilas ei kuitenkaan huomaa katkoksia, koska apteekit voivat toimittaa vastaavan vaihtokelpoisen valmisteen. Lääkeyrityksillä eli myyntiluvan haltijoilla on lakisääteinen velvollisuus varmistaa, että myyntiluvan saaneet valmisteet ovat jatkuvasti tukkukauppojen ja apteekkien saatavilla potilaiden tarpeisiin.
Fimean rooli ja tavoitteet
Fimean tehtävänä on lääkkeiden sekä niiden valmistuksen ja jakelun asianmukaisuuden varmistaminen. Fimea myöntää myyntilupia ihmis- ja eläinlääkkeille sekä valvoo lääkinnällisten laitteiden ja ihmisperäisten aineiden vaatimustenmukaisuutta ja alan toimijoita Suomessa. Lisäksi Fimea varmistaa apteekkipalveluiden riittävyyttä, lääkkeiden toimitus- ja jakeluvarmuutta sekä hintakilpailun toimivuutta kuluttajan aseman turvaamiseksi.
Fimean tavoitteena on edistää kestävällä tavalla kansalaisten terveyttä ja hyvinvointia. Lisäksi tavoitteena on, että turvalliset, laadukkaat sekä edulliset lääkkeet ja lääkinnälliset tuotteet ovat kansalaisten saatavilla, kun niitä tarvitaan. Fimea pyrkii olemaan ensisijainen ja ajantasainen tiedonlähde saatavuushäiriöistä. Tavoitteena on, että lääkkeiden ja lääkinnällisten tuotteiden saatavuushäiriöt vaikuttaisivat kansallisella tasolla potilashoitoihin mahdollisimman vähän.
Miten tavoitteiden saavuttamista edistetään Fimeassa?
Fimea toimii Euroopan lääkeviraston (EMA) koordinoimien keskitettyjen myyntilupien raportointi- ja rinnakkaisraportointitehtävissä merkittävällä panoksella. Erityisen vahvaa asiantuntemusta on biosimilaarien sekä syöpä- ja autoimmuunisairauksien hoitoon tarkoitettujen valmisteiden arvioinnissa.
Eläinlääkkeiden osalta Fimea osallistuu aktiivisesti uusien myyntilupien arviointiin erityisesti omilla painopistealueillaan, kuten tarttuvien eläintautien rokotteiden arviointiin. Tärkeänä painopisteenä eläinlääkearvioinneissa ovat myös innovatiiviset, uudet biologiset valmisteet.
| Lääkevalmiste Järjestä taulukko sarakkeen mukaan nousevasti | 2021 Järjestä taulukko sarakkeen mukaan nousevasti | 2022 Järjestä taulukko sarakkeen mukaan nousevasti | 2023 Järjestä taulukko sarakkeen mukaan nousevasti | 2024 Järjestä taulukko sarakkeen mukaan nousevasti | 2025 Järjestä taulukko sarakkeen mukaan nousevasti |
|---|---|---|---|---|---|
| Ihmislääke | 9 867 | 10 059 | 10 311 | 10 757 | 11 324 |
| Eläinlääke | 1 163 | 1 192 | 1 215 | 1 278 | 1 367 |
| Yhteensä | 10 715 | 11 030 | 11 252 | 11 526 | 12 035 |
Erityisluvat osana lääkkeiden saatavuuden turvaamista
Lääkeyritykset vastaavat lääkkeiden saatavuudesta ja niiden tuomisesta markkinoille. Fimea puolestaan valvoo tilannetta ja selvittää mahdollisia saatavuushäiriöitä yhteistyössä yritysten kanssa. Fimea ylläpitää verkkosivuillaan ajankohtaista luetteloa saatavuushäiriöistä ja tiedottaa tarvittaessa erillisillä verkkotiedotteilla. Saatavuuteen liittyvää tietoa jaetaan myös säännöllisesti lääkealan toimijoille, sosiaali- ja terveysministeriölle sekä EU:n ja Pohjoismaiden lääkeviranomaisille.
Fimea myöntää erityis- tai poikkeuslupia tilanteissa, joissa kriittistä myyntiluvallista lääkevalmistetta ei ole saatavilla Suomessa. Erityislupapäätösten määrä kasvoi vuonna 2025, koska osa aiemmin määräaikaisilla erityisluvilla käytössä olleista valmisteista siirtyi potilas‑ tai laitoskohtaisen erityisluvan piiriin. Näitä valmisteita on aiemmin voitu luovuttaa kulutukseen ilman erillistä erityislupahakemusta, mikä on voinut kentällä luoda virheellisen käsityksen siitä, että valmisteet olisivat Fimean arvioimia laadun, turvallisuuden ja tehokkuuden osalta. Tämän seurauksena ensisijaisena hoitona on voitu käyttää Suomessa myyntiluvatonta valmistetta, vaikka potilaan hoito tulisi ensisijaisesti toteuttaa myyntiluvallisella lääkevalmisteella. Erityislupahakemusmenettely selkeyttää lääkärille valmisteen asemaa ja korostaa erityisluvan poikkeuksellista luonnetta lääkehoidon toteutuksessa.
| Suorite Järjestä taulukko sarakkeen mukaan nousevasti | 2021 Järjestä taulukko sarakkeen mukaan nousevasti | 2022 Järjestä taulukko sarakkeen mukaan nousevasti | 2023 Järjestä taulukko sarakkeen mukaan nousevasti | 2024 Järjestä taulukko sarakkeen mukaan nousevasti | 2025 Järjestä taulukko sarakkeen mukaan nousevasti |
|---|---|---|---|---|---|
| Saatavuushäiriöilmoitukset | 1 527/ 183 |
2 184/ 151 |
2 710/ 139 |
2 519/ 157 |
2 585/ 198 |
| Velvoitevarastointipäätökset | 297/12 | 466/11 | 480/14 | 472/14 | 430/19 |
| Velvoitevarastoinnin alituslupapäätökset | 258/12 | 431/10 | 437/13 | 434/14 | 387/19 |
| Saapuneet poikkeuslupahakemukset | 125/49 | 175/60 | 200/46 | 274/20 | 231/21 |
| Poikkeuslupapäätökset* | 107/46 | 152/53 | 186/39 | 254/19 | 206/20 |
| Potilaskohtaiset erityislupapäätökset | 6 809/ 176 |
7 402/ 123 |
8 917/ 68 |
8 805/ 75 |
15 145/ 190 |
| Laitoskohtaiset erityislupapäätökset | 7 730/ 738 |
8 019/ 678 |
7 926/ 554 |
7 598/ 592 |
7 178/ 883 |
| Määräaikaiset erityislupapäätökset | Puuttuu/58 | 110/71 | 81/92 | 74/74 | 55/62 |
| Lääkinnällisten laitteiden saatavuusilmoitukset (artikla 10a)** | 26 | ||||
| Lääkinnällisiin laitteisiin liittyvät poikkeusluvat (MD-asetus ja IVD-asetus) | 1 | 14 | 10 | 6 | 6 |
Fimea seuraa eri suoritteita, jotka vaikuttavat lääkkeiden saatavuuteen, esimerkiksi saatavuushäiriöilmoituksia, lääkevalmisteiden velvoitevarastoinnin alituslupamääriä sekä poikkeuslupa- ja erityislupamääriä.
* Poikkeuslupien osalta laskentatapa on muuttunut, minkä vuoksi vuoden 2022 jälkeiset lukemat eivät ole suoraan vertailukelpoisia aikaisempien vuosien määriin.
** Muutosasetuksen (EU) 2024/1860 artikla 10a on 10.1.2025 alkaen velvoittanut lääkinnällisen laitteen valmistajaa ilmoittamaan, jos on kohtuudella ennakoitavissa, että toimitusten keskeytyminen tai lakkaaminen voisi aiheuttaa potilaille tai kansanterveydelle vakavaa haittaa tai vakavan haitan vaaraa.
Lääkkeiden (ihmis-/eläinlääkkeet) ja lääkinnällisten laitteiden saatavuuden hallintaan liittyvien suoritteiden lukumäärät vuosina 2021-2025 saavutettavassa muodossa (pdf).
-
Fimea käsitteli viime vuonna yli 23 000 erityislupahakemusta lääkkeille, joilla ei ole myyntilupaa Suomessa. Prosessi oli aiemmin paperikeskeinen ja hidas, minkä vuoksi sähköistämistarve tunnistettiin jo pitkään. Uudistustyön tuloksena otettiin käyttöön ERKKA-järjestelmä (erityislupien rekisteri ja asiointijärjestelmä) vuoden 2025 aikana. Sähköinen asiointipalvelu avattiin 4.2.2025 ja samalla Fimean verkkosivujen lääkehaku päivitettiin sisältämään erityislupaa edellyttävät valmisteet. ERKKA koostuu kahdesta pääosasta: asiointipalvelusta hakijoille (lääkärit, hammaslääkärit, eläinlääkärit, apteekit ja lääketukkukaupat) sekä rekisteriosasta viranomaiskäsittelyyn Fimeassa.
Sähköinen asiointi poisti paperivaiheet
Sähköinen asiointi sujuvoitti erityisluvan hakemista: hakemusten laatiminen, käsittely ja päätöksen jakelu tapahtuvat nyt alusta loppuun digitaalisesti ilman paperivaiheita. Kaikki hakemukset ja päätökset hallinnoidaan yhdessä järjestelmässä sekä ihmisten että eläinten lääkinnässä. Hakemus tehdään sähköisellä lomakkeella, ja päätös tulee nähtäville asiointipalveluun heti, kun Fimea on sen tehnyt – kirjepostia ei enää tarvitse odottaa. Tämä on poistanut merkittävän viiveen lupaprosessista.
Järjestelmä nopeuttaa käsittelyä ja tukee työn hallintaa
ERKKAn käyttöönotto nopeutti ja selkeytti hakemusten käsittelyä. Järjestelmä ohjaa hakemuksen täyttämistä niin, että kaikki pakolliset tiedot tulee antaa ennen lähettämistä, mikä on vähentänyt puutteellisten hakemusten määrää. Valmiste valitaan lomakkeella suoraan listasta, jolloin hakemus kohdistuu yksiselitteisesti oikeaan valmisteeseen. Lisäselvityspyyntöjen tarve on vähentynyt, sillä automaattinen tietojen täsmäytys poistaa monia kysymyksiä – aiemmin hakijoilta pyydettiin usein täydennyksiä lääkevalmisteen tarkemmista tiedoista.
Myös työnkulun hallinta on parantunut: Fimean käsittelijät näkevät sähköisestä työjonosta helposti kaikkien vireillä olevien ja saapuneiden hakemusten tilanteen ja prosessi on nyt läpinäkyvämpi ja hallittavampi Fimeassa.
Suurin osa hakemuksista tulee ERKKAn kautta, mutta osa saapuu yhä myös asiointijärjestelmän ulkopuolella, esimerkiksi turvapostilla. Nämäkin hakemukset tallennetaan ERKKA-järjestelmään, jolloin kaikki hakemukset ovat yhdessä paikassa käsittelijöiden löydettävissä sähköisessä työjonossa.
Käyttäjäpalaute vie palvelua eteenpäin
Käyttäjäkokemukset ovat olleet suurelta osin myönteisiä. Sähköinen asiointi on saanut kiitosta helppokäyttöisyydestä, visuaalisesta selkeydestä ja nopeudesta. Hakijoille merkittävää on, että hakemuksen tila näkyy reaaliaikaisesti ja päätösasiakirja on ladattavissa palvelusta heti, kun lupa on myönnetty. Erityisesti hakemuskäsittelyn nopeus on huomattu – kiireellisissä tapauksissa päätöksen saa usein samana tai seuraavana päivänä.
Palautteen perusteella ERKKA-palvelua kehitettiin edelleen. Käyttäjät toivat esiin joitakin käytettävyyshaasteita ja toiveita. Palvelun löydettävyyttä parannettiin Fimean sivuilla: luotiin uusi Sähköinen asiointi -pääsivu ja erityislupasivujen ylävalikkoon lisättiin selkeä painike ERKKA-palveluun. Viestintää palvelusta laajennettiin ja ohje- sekä erityislupiin liittyvät verkkosivut päivitettiin. Usein kysytyt kysymykset -osio laajennettiin, jotta hakijat löytävät tarvitsemansa tiedot helpommin.
Yhteenvetona ERKKA-järjestelmä on tuonut merkittäviä parannuksia erityislupaprosessiin: hakemusten käsittely on nopeutunut, tieto kulkee digitaalisesti ja järjestelmä ohjaa hakemuksen täyttämistä, mikä vähentää virheitä ja lisäselvityspyyntöjä. Prosessi on nyt hallittavampi ja läpinäkyvämpi sekä Fimealle että hakijoille. Käyttäjäkokemukset osoittavat, että sähköinen asiointi vastaa alan tarpeisiin ja palvelua kehitetään aktiivisesti palautteen pohjalta. Selkeä järjestelmä ja ohjeistus tukevat sujuvaa hakemusprosessia, ja lopputuloksena erityislupien käsittely on muuttunut nykyaikaiseksi ja tehokkaaksi.
Fimea kehitti ennakoivaa varautumista tukevia tietojärjestelmiä
Fimea kehitti Saatavuus ja varautuminen ‑raportointityökalun (SaVa), joka kokoaa saatavuuden tilannekuvan muodostamiseen tarvittavat tiedot yhdelle alustalle ja mahdollistaa niiden yhdistelemisen sekä aiempaa tehokkaamman hyödyntämisen. Työkaluun toteutettiin saatavuuteen vaikuttavien erilaisten signaalien seuranta sekä niiden riskiluokan arviointi. Projektin yhteydessä työkaluun integroitiin myös Velvoitevarastointi- sekä Saatavuuden seuranta (Sasse) -sovellukset. SaVan tavoitteena on tukea siirtymistä reaktiivisesta toimintatavasta ennakoivaan toimintamalliin.
Fimea osallistui EU‑tason sääntelyn valmisteluun lääkepulan ehkäisemiseksi
Kriittisten lääkkeiden asetus (Critical Medicines Act, CMA) on Euroopan komission maaliskuussa 2025 antama ehdotus uudeksi EU-asetukseksi, jonka tavoitteena on parantaa keskeisten lääkkeiden saatavuutta ja toimitusvarmuutta koko unionissa. Asetus velvoittaa jäsenvaltiot ja myyntiluvan haltijat tehostettuun ennakointiin, raportointiin ja lääkepulan ehkäisyyn, tukee investointeja EU-alueen tuotantoon, helpottaa yhteishankintoja sekä kannustaa toimitusketjujen monipuolistamiseen, jotta potilaat saisivat tarvitsemansa lääkehoidot luotettavammin myös häiriötilanteissa. Fimea osallistui aktiivisesti asetuksen taustatyöskentelyyn.
Apteekkivalvonnassa edistettiin edullisempien lääkkeiden saatavuutta
Vuonna 2025 yhtenä Fimean apteekkivalvonnan painopistealueena oli edullisimpien lääkevalmisteiden saatavuuden arviointi apteekkitarkastusten yhteydessä. Taustalla oli vuoden alussa voimaan tullut lakisääteinen velvoite, jonka mukaan apteekkien on pidettävä varastossaan edullisimpia lääkevalmisteita sekä resepti‑ että itsehoitolääkkeistä. Lisäksi apteekit velvoitettiin antamaan asiakkaille tietoa lääkkeiden hinnoista ja tarjoamaan aina ensin tosiasiallisesti edullisinta valmistetta. Hinnaltaan edullisempien lääkevalmisteiden käyttö hyödyttää paitsi yhteiskuntaa taloudellisesti myös väestöä terveydellisesti, koska useammalla lääkkeen käyttäjällä on varaa hankkia tarvitsemansa lääkkeet.
| Summa Järjestä taulukko sarakkeen mukaan nousevasti | 2020 Järjestä taulukko sarakkeen mukaan nousevasti | 2021 Järjestä taulukko sarakkeen mukaan nousevasti | 2022 Järjestä taulukko sarakkeen mukaan nousevasti | 2023 Järjestä taulukko sarakkeen mukaan nousevasti | 2024 Järjestä taulukko sarakkeen mukaan nousevasti |
|---|---|---|---|---|---|
| Yhteensä, milj. euroa | 75,1 | 78,2 | 102,3 | 114,8 | 113,1 |
| Säästö/vaihto, euroa | 18,2 | 16,7 | 21,2 | 23,2 | 22,7 |
Lähteet: Suomen lääketilasto 2024. Kelan aineisto "Sairausvakuutuksesta korvattavat lääketoimitukset". Hinta- ja viitehintatiedot Lääketietokannan tiedoista. Korvaukset sisältävät lisäkorvaukset. Tilasto kattaa myös ennen alkuomavastuun täyttymistä tehdyt ostot.
Lääkkeen vaihtamisen tuomat säästöt vuosina 2020–2024 saavutettavassa muodossa (pdf).
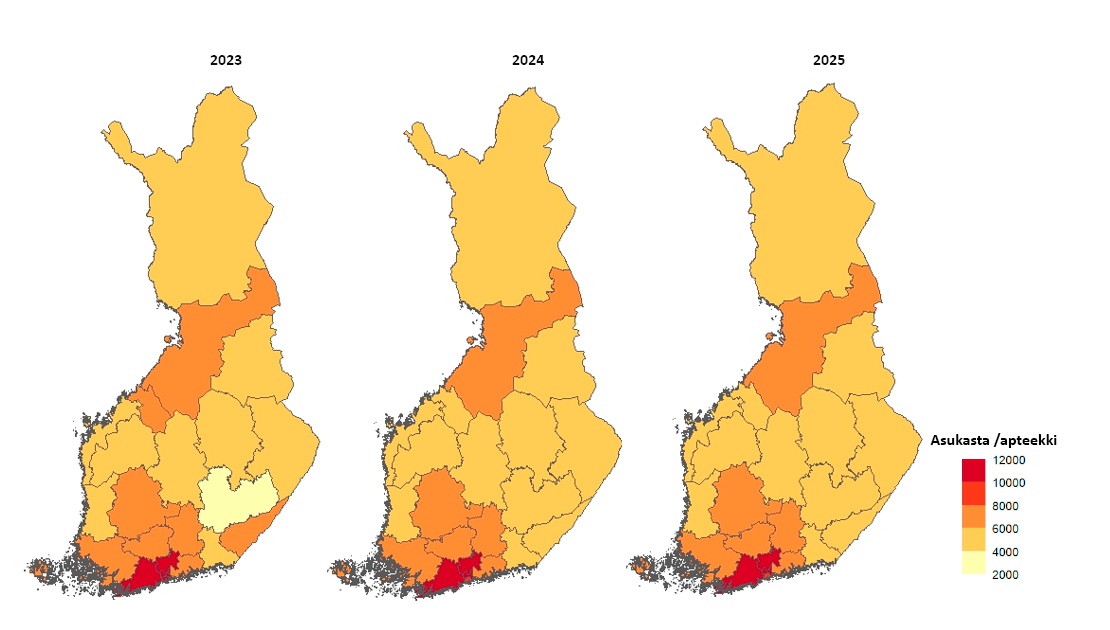
Apteekkiverkkoa kehitettiin apteekkipalvelujen saatavuuden turvaamiseksi
Apteekkien ja erityisesti niiden alaisuudessa oikeutena toimivien sivuapteekkien määrä pieneni vuoden 2025 aikana. Ainakin osittain tähän vaikuttivat odotettavissa olevat apteekkitoimintaan kohdistuvat säästötoimet. Varmistaakseen apteekkipalvelujen saatavuuden Fimea muutti joitain pienimpiä itsenäisiä apteekkeja sivuapteekeiksi tilanteissa, joissa itsenäiselle apteekille ei enää ollut toimintaedellytyksiä. Fimea myös perusti yksittäisiä uusia apteekkeja ja uudelleenmääritteli apteekkien sijaintialuerajoja siten, että apteekkipalveluja olisi saatavilla juuri siellä, missä niitä tarvitaan.
Pakkausmerkintöjen kielivaatimuksiin tehtiin joustoja saatavuuden parantamiseksi
Lääkelainsäädäntö edellyttää kansallisten kielten käyttöä pakkausmerkinnöissä. Maaliskuusta 2025 alkaen lääkeyritykset ovat voineet hakea Regulatory flexibility for common Nordic packages -hankkeen kautta yhteispohjoismaisia sairaalavalmisteiden lääkepakkauksia englanninkielisin tekstein. Myös pohjoismaisten sairaalavalmisteiden pakkauksissa ensisijainen vaihtoehto ovat kansalliset kielet, mutta hyvin pienimenekkisiä, kriittisiä valmisteita ei kansallisilla kielillä vaadittuna saada aina tarjolle.
Vuoden lopussa saatavuuden turvaamista helpotettiin sallimalla englannin kielen lisäksi pakkauksiin tarvittaessa myös muita EU-kieliä. Tällä muutoksella pystyttiin merkittävästi laajentamaan mahdollisuuksia saada Suomeen käyttöön joitakin hyvin pienimenekkisiä sairaalavalmisteita.
Hankkeen myötä hyväksyttiin 2025 aikana englanninkieliset pakkaukset 21 sairaalavalmisteelle.
Fimea turvasi eläinlääkkeiden saatavuutta häiriötilanteissa
Eläinlääkkeiden saatavuushäiriöt ovat globaali ongelma, joka korostuu Suomen kaltaisella pienellä markkina-alueella. Fimea jatkoi vuonna 2025 toimia saatavuushäiriöiden ennaltaehkäisemiseksi ja tarkasteli muun muassa mahdollisuuksia poiketa pakkausten kielivaatimuksista hallitusti.
Vuonna 2025 merkittäviä ja pitkäkestoisia saatavuushäiriöitä ilmeni esimerkiksi seuraavissa eläinlääkkeissä:
- Kalankasvatuksessa käytettävä formaliini, jonka saatavuus estyi, koska eläinlääkettä ei saatu Suomeen eivätkä muut vaihtoehdot olleet elinkeinolle soveltuvia. Tilannetta käsiteltiin usean viranomaisen ja toimialan yhteistyönä, ja kalankasvatuksen toiminta turvattiin lopulta väliaikaisratkaisulla. Pidemmällä aikavälillä tavoitteena on, että myös Suomeen saadaan myyntiluvallinen eläinlääke.
- Koirille tarkoitettu kaliumbromidi, jonka saatavuushäiriö oli EU:n laajuinen ja koski ainoita kahta EU:ssa myyntiluvallista eläinlääkettä. Korvaavina valmisteina käytettiin ex tempore -valmisteita sekä erityisluvallista EU:n ulkopuolista eläinlääkettä.
- Hevosille tarkoitetut influenssa‑ ja jäykkäkouristusrokotteet (Suomessa kaksi eniten käytettyä), joilla oli lähes koko vuoden 2025 ajan kestänyt saatavuushäiriö. Häiriöitä voitiin paikata muilla vastaavilla myyntiluvallisilla valmisteilla.
-
Huhtikuussa 2024 käynnistynyt biologisten lääkkeiden lääkevaihto laajeni vuonna 2025 kahteen otteeseen, ja samalla valmistauduttiin viimeiseen vuoden 2026 alussa tapahtuneeseen käyttöönottovaiheeseen.
Lääkäreillä on ollut jo vuodesta 2017 alkaen velvollisuus määrätä edullisinta potilaan hoitoon soveltuvaa biologista lääkettä. Biologisten lääkkeiden lääkevaihdon käyttöönotto on mahdollistanut lääkkeen vaihdon edullisempaan valmisteeseen myös apteekissa.
Biologisten lääkkeiden lääkevaihto apteekeissa käynnistyi huhtikuussa 2024, kun laskimotukosten estoon ja hoitoon käytettävät enoksapariinivalmisteet tulivat ensimmäisinä biologisina lääkkeinä apteekissa toteutettavan lääkevaihdon piiriin. Tammikuussa 2025 lääkevaihto laajeni insuliineja lukuun ottamatta kaikkiin muihin biologisiin lääkkeisiin, joilla hoidetaan esimerkiksi reumaa, psoriasista, astmaa ja tulehduksellisia suolistosairauksia.
Diabeteksen hoidossa käytettäviin insuliineihin lääkevaihto laajeni kahdessa erässä. Glargininsuliinien lääkevaihto alkoi 1.4.2025. Muihin pitkävaikutteisiin insuliineihin lääkevaihto laajeni vuoden 2026 alussa. Lyhytvaikutteiset insuliinit eivät kuulu lääkevaihdon piiriin, eikä alle 18-vuotiaiden potilaiden biologisia lääkkeitä vaihdeta apteekissa.
Lääkealan turvallisuus- ja kehittämiskeskus Fimean näkökulmasta biologisten lääkkeiden lääkevaihdon käyttöönotto on edennyt ennakoidusti ja hallitusti.
Biologisten lääkkeiden lääkevaihto on tuonut säästöjä
Biologisten lääkkeiden lääkevaihdolla on haluttu lisätä hintakilpailua ja vähentää lääkekorvauskustannuksia. Kelan julkaisemien tietojen mukaan biologisten lääkkeiden hintakilpailua edistävät toimet näyttävät toimineen ja alentaneen korvauskustannuksia merkittävästi. Kelan joulukuussa 2025 julkaisemien ennakkoarvioiden mukaan niiden biologisten lääkkeiden lääkekorvausmenot, joille löytyy biosimilaari, tulevat olemaan vuonna 2025 noin 41 miljoonaa euroa pienemmät kuin vuonna 2022. Kelan joulukuinen tarkastelu koski tammi–syyskuuta 2025, jolloin vaihdon piirissä olivat olleet kaikki muut biologiset lääkkeet kuin insuliinit. Huhti–syyskuun 2025 ajalta mukana tarkastelussa olivat myös huhtikuussa vaihdon piiriin tulleet glargininsuliinit.
Laiteneuvonnalla varmistetaan turvallinen lääkevaihto
Biologinen lääke on valmiste, jonka vaikuttava aine on biologinen aine. Biologinen lääke annetaan yleensä infuusiona laskimoon tai pistoksena ihon alle. Biologisten lääkkeiden lääkemääräykset ovat voimassa vain vuoden kerrallaan.
Biosimilaari on yhtä tehokas ja yhtä turvallinen kuin alkuperäinen biologinen lääke. Se sisältää samaa vaikuttavaa ainetta kuin alkuperäislääke. Fimea määrittelee keskenään vaihtokelpoiset biologiset lääkkeet neljä kertaa vuodessa. Fimean lääkehaun avulla voi tarkistaa, mitkä lääkkeet ovat biologisia lääkkeitä.
Alkuperäisen biologisen lääkkeen ja biosimilaarin antolaitteiden toiminta voi erota toisistaan. Vaihtokelpoisten valmisteiden antolaitteet ovat kuitenkin siinä määrin samankaltaisia, että vaihto voidaan toteuttaa turvallisesti apteekin farmaseuttisen henkilökunnan antaman laiteneuvonnan jälkeen.
Fimea julkaisi käyttöönottovaiheen aikana heinäkuussa 2024 biologisten lääkkeiden laite-eroja koostavan hakupalvelun apteekkien lääkeneuvonnan tueksi. Hakupalveluun on koottu vain keskeisimmät tiedot lääkevalmisteista ja niiden laite-eroista. Hakuun on koottu kaikki ne inhalaatiovalmisteet ja biologiset lääkkeet, joille Fimea on tuottanut lääkevaihdon lisätietoja.
Lue lisää
Kelan tutkimusblogi: Biologisten lääkkeiden hintakilpailu säästää kymmeniä miljoonia