Antalet försäljningstillstånd (giltiga försäljningstillstånd) 2021-2025 i tillgänglig form (PDF).
Främjande av tillgången till läkemedel och medicintekniska produkter

FN:s mål 3 för hållbar utveckling:

3.4 Genom förebyggande insatser och behandling fram till 2030 minska antalet människor som dör i förtid av icke smittsamma sjukdomar med en tredjedel samt främja psykisk hälsa och välbefinnande.
3.8 Skapa tillgång till allmän hälso- och sjukvård som även skyddar mot ekonomiska risker, tillgång till högkvalitativa och väsentliga hälso- och sjukvårdstjänster samt säkra, effektiva, högklassiga och förmånliga nödvändiga läkemedel och vaccinationer för alla.
Utmaning
Dödligheten i anslutning till kroniska sjukdomar, såsom hjärt- och kärlsjukdomar, cancer, diabetes och sjukdomar i andningsorganen, är fortfarande en central hälsoindikator internationellt sett. I Finland betraktas dessa sjukdomar som betydande folksjukdomar, och ändamålsenlig läkemedelsbehandling i rätt tid är en väsentlig del av hanteringen av symtomen, fördröjningen av sjukdomarnas framskridande och förbättringen av livskvaliteten.
Den globala verksamhetsmiljön medför ständigt utmaningar i anslutning till tillgången till läkemedel och medicintekniska produkter. Störningar kan uppstå till exempel på grund av världspolitiska spänningar, problem med tillgången på råvaror, sårbarheter i produktionskedjorna och snabba förändringar i efterfrågan på marknaden. Oftast märker patienten dock inte avbrotten, eftersom apoteken kan expediera ett motsvarande utbytbart preparat. Läkemedelsföretagen, dvs. innehavarna av försäljningstillstånd, har en lagstadgad skyldighet att säkerställa att de preparat som beviljats försäljningstillstånd ständigt är tillgängliga för grossister och apotek för patienternas behov.
Fimeas roll och mål
Fimeas uppgift är att säkerställa att läkemedlen samt tillverkningen och distributionen av dem är ändamålsenlig. Fimea beviljar försäljningstillstånd för humanläkemedel och veterinärmedicinska läkemedel samt övervakar att medicintekniska produkter och ämnen med humant ursprung överensstämmer med kraven och övervakar aktörer inom branschen i Finland. Dessutom säkerställer Fimea att apotekstjänsterna är tillräckliga, att läkemedlen levereras och distribueras säkert samt att priskonkurrensen fungerar för att trygga konsumentens ställning.
Fimea har som mål att på ett hållbart sätt främja medborgarnas hälsa och välfärd. Dessutom är målet att säkra, högklassiga och förmånliga läkemedel och medicintekniska produkter ska vara tillgängliga för medborgarna när de behövs. Fimea strävar efter att vara den primära och aktuella informationskällan när det gäller störningar i tillgången. Målet är att störningar i tillgången till läkemedel och medicintekniska produkter ska påverka patientbehandlingarna så lite som möjligt på nationell nivå.
Hur främjar Fimea att målen uppnås?
Fimea bidrar i betydande utsträckning till rapporterings- och parallellrapporteringsuppgifter inom de centralt koordinerade godkännandeförfaranden som leds av Europeiska läkemedelsmyndigheten (EMA). Särskilt stark kompetens finns inom utvärdering av biosimilarer samt läkemedel avsedda för behandling av cancer och autoimmuna sjukdomar.
När det gäller veterinärläkemedel deltar Fimea aktivt i bedömningen av nya försäljningstillstånd, särskilt inom sina egna prioriterade områden, såsom utvärdering av vacciner mot smittsamma djursjukdomar. Ett viktigt fokusområde inom veterinärläkemedelsbedömningarna är även innovativa, nya biologiska läkemedel.
| Läkemedelspreparat Sort the table ascending by the column | 2021 Sort the table ascending by the column | 2022 Sort the table ascending by the column | 2023 Sort the table ascending by the column | 2024 Sort the table ascending by the column | 2025 Sort the table ascending by the column |
|---|---|---|---|---|---|
| Humanläkemedel | 9 867 | 10 059 | 10 311 | 10 757 | 11 324 |
| Veterinärmedicinskt läkemedel | 1 163 | 1 192 | 1 215 | 1 278 | 1 367 |
| Sammanlagt | 11 030 | 11 252 | 11 526 | 12 035 | 12 035 |
Specialtillstånd som en del av tryggandet av tillgången till läkemedel
Läkemedelsföretagen ansvarar för tillgången till läkemedel och införandet av dem på marknaden. Fimea övervakar situationen och utreder eventuella störningar i tillgången i samarbete med företagen. Fimea upprätthåller en aktuell förteckning över störningar i tillgången till läkemedel på sin webbplats och informerar vid behov med separata webbmeddelanden. Information i anslutning till tillgången delas också regelbundet ut till aktörer inom läkemedelsområdet, social- och hälsovårdsministeriet samt läkemedelsmyndigheterna i EU och de nordiska länderna.
Fimea beviljar special- eller undantagstillstånd i situationer där ett kritiskt läkemedelspreparat med försäljningstillstånd inte finns att tillgå i Finland. Antalet beslut om specialtillstånd ökade 2025, eftersom en del av de preparat som tidigare användes med temporära specialtillstånd övergick till att omfattas av patient- eller institutionsspecifika specialtillstånd. Dessa preparat har tidigare kunnat överlåtas till förbrukning utan separat ansökan om specialtillstånd, vilket på fältet har kunnat skapa en felaktig uppfattning om att preparaten skulle ha bedömts av Fimea i fråga om kvalitet, säkerhet och effektivitet. Till följd av detta har man som primär behandling kunnat använda preparat som saknar försäljningstillstånd i Finland, även om vården av patienten i första hand borde genomföras med ett läkemedelspreparat med försäljningstillstånd. Förfarandet för ansökan om specialtillstånd förtydligar preparatets ställning för läkaren och betonar specialtillståndets exceptionella karaktär i genomförandet av läkemedelsbehandlingen.
| Prestation Sort the table ascending by the column | 2021 Sort the table ascending by the column | 2022 Sort the table ascending by the column | 2023 Sort the table ascending by the column | 2024 Sort the table ascending by the column | 2025 Sort the table ascending by the column |
|---|---|---|---|---|---|
| Anmälningar om störningar i tillgången | 1 527/183 | 2 184/151 | 2 710/139 | 2 519/157 | 2 585/198 |
| Beslut om obligatorisk lagring | 297/12 | 466/11 | 480/14 | 472/14 | 430/19 |
| Beslut om rätt att få underskrida lagervolymen vid obligatorisk lagring | 258/12 | 431/10 | 437/13 | 434/14 | 387/19 |
| Ansökningar om undantagstillstånd | 125/49 | 175/60 | 200/46 | 274/20 | 231/21 |
| Beslut om undantagstillstånd* | 107/46 | 152/53 | 186/39 | 254/19 | 206/20 |
| Beslut om patientspecifika specialtillstånd | 6 809/176 | 7 402/123 | 8 917/68 | 8 805/75 | 15 145/190 |
| Beslut om anläggningsspecifika specialtillstånd | 7 730/738 | 8 019/678 | 7 926/554 | 7 598/592 | 7 178/883 |
| Tidsbundna beslut om specialtillstånd | Saknas/58 | 110/71 | 81/92 | 74/74 | 55/62 |
| Tillgänglighetsanmälningar för medicintekniska produkter (artikel 10a) | 26 | ||||
| Undantagstillstånd för medicintekniska produkter (MD-förordningen och IVD-förordningen) | 1 | 14 | 10 | 6 | 6 |
Fimea följer upp olika prestationer som påverkar tillgången till läkemedel, till exempel anmälningar om störningar i tillgången, antalet tillstånd att underskrida den obligatoriska lagringen av läkemedelspreparat samt antalet undantagstillstånd och specialtillstånd.
* I fråga om undantagstillstånd har beräkningssättet ändrats och därför är siffrorna efter 2022 inte direkt jämförbara med tidigare års antal.
** Artikel 10a i ändringsförordningen (EU) 2024/1860 har från och med 10.1.2025 ålagt tillverkaren av en medicinteknisk produkt att meddela om det rimligen kan förutses att avbrott i eller upphörande av leveranserna kan orsaka allvarliga olägenheter för patienter eller folkhälsan eller risk för allvarlig olägenheter.
Antalet prestationer i anslutning till hantering av tillgången till läkemedel och medicintekniska produkter 2021–2025 i tillgänglig form (PDF).
-
Fimea behandlade i fjol över 23 000 ansökningar om specialtillstånd för läkemedel som inte har försäljningstillstånd i Finland. Processen var tidigare papperscentrerad och långsam och därför identifierades behovet av en e-tjänst redan länge. Som ett resultat av reformen togs ERKKA-systemet (registret över och e-tjänsten för specialtillstånd) i bruk under 2025. E-tjänsten öppnades 4.2.2025 och samtidigt uppdaterades läkemedelssökningen på Fimeas webbplats så att den innehåller preparat som kräver specialtillstånd. ERKKA består av två huvuddelar: e-tjänsten för sökande (läkare, tandläkare, veterinärer, apotek och läkemedelspartiaffärer) samt registerdelen för myndighetsbehandling vid Fimea.
Elektronisk ärendehantering avskaffade pappersstegen
Den elektroniska ärendehanteringen gjorde det smidigare att ansöka om specialtillstånd: utarbetandet, behandlingen och delningen av ansökningar sker nu digitalt från början till slut utan papperssteg. Alla ansökningar och beslut administreras i ett system i fråga om läkemedel för både människor och djur. Ansökan görs med en elektronisk blankett och beslutet läggs fram i e-tjänsten genast när Fimea har fattat ett beslut, man behöver inte längre vänta på brevpost. Detta har avlägsnat en betydande fördröjning i tillståndsprocessen.
Systemet påskyndar behandlingen och stöder hanteringen av arbetet
Ibruktagandet av ERKKA påskyndade och underlättade behandlingen av ansökningarna. Systemet styr ifyllandet av ansökan så att alla obligatoriska uppgifter ska ges innan ansökan skickas, vilket har minskat antalet bristfälliga ansökningar. Preparatet väljs direkt från en lista till blanketten, varvid ansökan entydigt gäller rätt preparat. Behovet av tilläggsutredningar har minskat, eftersom den automatiska avstämningen av uppgifterna avlägsnar många frågor – tidigare bad man sökandena ofta om kompletteringar och närmare uppgifter om läkemedelspreparatet.
Hanteringen av arbetsflödet har också förbättrats: Fimeas handläggare ser lätt situationen för alla anhängiga och inkomna ansökningar i den elektroniska arbetskön och processen är nu mer transparent och hanterbar vid Fimea.
Största delen av ansökningarna inkommer via ERKKA, men en del kommer fortfarande även utanför e-tjänsten, till exempel med krypterad e-post. Även dessa ansökningar sparas i ERKKA-systemet, varvid handläggarna kan hitta alla ansökningar på ett ställe i den elektroniska arbetskön.
Användarrespons för tjänsten vidare
Användarupplevelserna har till stor del varit positiva. E-tjänsten har fått beröm för att den är lätt att använda, visuellt tydlig och snabb. Det är viktigt för sökandena att ansökans status visas i realtid och att beslutshandlingen kan laddas ner från tjänsten genast när tillståndet har beviljats. I synnerhet snabbheten i behandlingen av ansökningarna har uppmärksammats – i brådskande fall får man ofta ett beslut samma eller följande dag.
Utifrån responsen vidareutvecklades ERKKA-tjänsten. Användarna lyfte fram några brister i användbarheten och önskemål. Tjänsten gjordes lättare att hitta på Fimeas webbplats: en ny huvudsida E-tjänst skapades och i den övre menyn på specialtillståndssidorna tillades en tydlig knapp till ERKKA-tjänsten. Kommunikationen om tjänsten utvidgades och webbplatsen för anvisningar och specialtillstånd uppdaterades. Avsnittet Vanliga frågor utvidgades så att de sökande lättare hittar den information de behöver.
Sammanfattningsvis har ERKKA-systemet medfört betydande förbättringar i processen för specialtillstånd: behandlingen av ansökningar har blivit snabbare, informationen förmedlas digitalt och systemet styr ifyllandet av ansökan, vilket minskar antalet fel och begäranden om tilläggsutredningar. Processen är nu mer hanterbar och transparent för både Fimea och de sökande. Användarupplevelserna visar att e-tjänsten motsvarar branschens behov och att tjänsten utvecklas aktivt utifrån responsen. Ett tydligt system och tydliga anvisningar stöder en smidig ansökningsprocess och slutresultatet är att behandlingen av specialtillstånd har blivit modern och effektiv.
Fimea utvecklade informationssystem som stöder föregripande beredskap
Fimea utvecklade rapporteringsverktyget Tillgänglighet och beredskap (Saatavuus ja varautuminen, SaVa), som sammanställer de uppgifter som behövs för att skapa en lägesbild på en plattform och gör det möjligt att kombinera och använda uppgifterna effektivare än tidigare. I verktyget genomfördes en uppföljning av olika signaler som påverkar tillgången samt en bedömning av deras riskklass. I samband med projektet integrerades också applikationerna Obligatorisk lagring och Uppföljning av tillgänglighet (Saatavuuden seuranta, Sasse) i verktyget. Målet med SaVa är att stöda övergången från ett reaktivt verksamhetssätt till en föregripande verksamhetsmodell.
Fimea deltog i beredningen av regleringen på EU-nivå för att förebygga läkemedelsbrist
Förordningen om kritiska läkemedel (Critical Medicines Act, CMA) är Europeiska kommissionens förslag till ny EU-förordning från mars 2025, vars mål är att förbättra tillgången till och leveranssäkerheten för centrala läkemedel i hela unionen. Förordningen förpliktar medlemsstaterna och innehavarna av försäljningstillstånd till effektiverare framförhållning, rapportering och förebyggande av läkemedelsbrist, stöder investeringar i produktion inom EU-området, underlättar gemensamma upphandlingar samt uppmuntrar till mångsidigare leveranskedjor så att patienterna får de läkemedelsbehandlingar de behöver på ett mer tillförlitligt sätt även i störningssituationer. Fimea deltog aktivt i bakgrundsarbetet till förordningen.
I apotekstillsynen främjades tillgången till förmånligare läkemedel
År 2025 var en av tyngdpunkterna i Fimeas apotekstillsyn en bedömning av tillgången till de förmånligaste läkemedelspreparaten i samband med apoteksinspektioner. I bakgrunden låg den lagstadgade skyldigheten som trädde i kraft i början av året, enligt vilken apoteken i sitt lager ska ha de förmånligaste läkemedelspreparaten av både recept- och egenvårdsläkemedel. Dessutom ålades apoteken att ge kunderna information om läkemedelspriserna och alltid först erbjuda det förmånligaste preparatet. Användningen av förmånligare läkemedelspreparat gynnar samhället, men också befolkningens hälsa, eftersom flera läkemedelsanvändare har råd att skaffa de läkemedel de behöver.
| Summa Sort the table ascending by the column | 2020 Sort the table ascending by the column | 2021 Sort the table ascending by the column | 2022 Sort the table ascending by the column | 2023 Sort the table ascending by the column | 2024 Sort the table ascending by the column |
|---|---|---|---|---|---|
| Totalt, miljoner euro | 75,1 | 78,2 | 102,3 | 114,8 | 113,1 |
| Besparing/byte, euro | 18,2 | 16,7 | 21,2 | 23,2 | 22,7 |
Källor: FPA:s (Folkpensionsanstalten) material Expedierade recept som ersätts av sjukförsäkringen. Pris- och referensprisuppgifter från uppgifterna i Läkemedelsdatabasen. Ersättningarna inkluderar tilläggsersättningar. Statistiken omfattar också inköp som gjorts innan initialsjälvrisken uppfyllts.
Besparingar som utbyte av läkemedel medfört 2020–2024 i tillgänglig form (PDF).
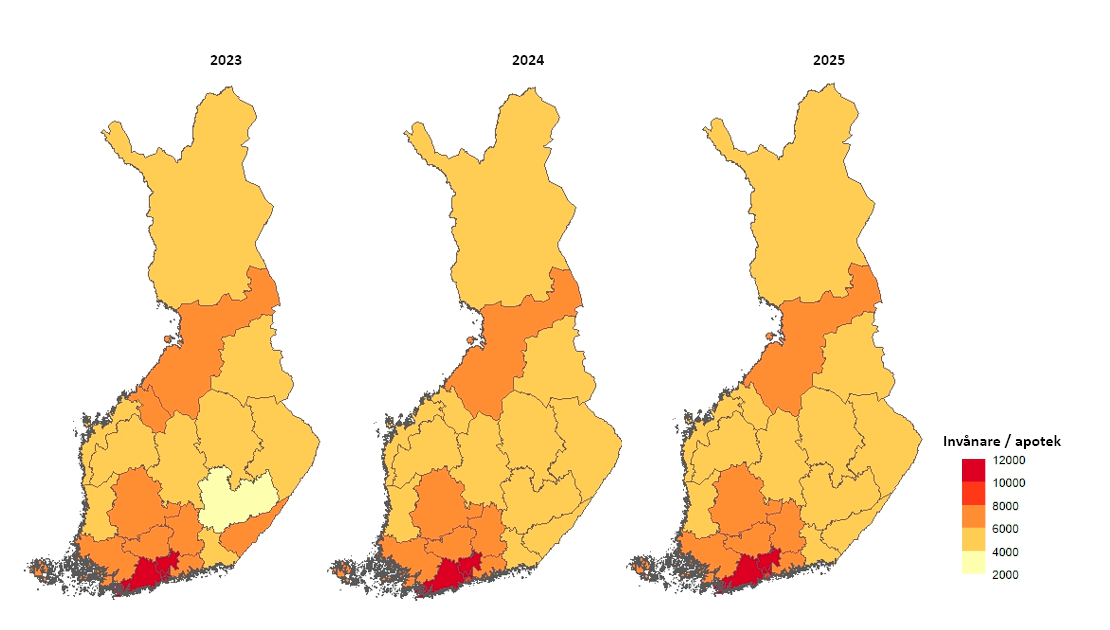
Apoteksnätet utvecklades för att trygga tillgången till apotekstjänster
Antalet apotek och i synnerhet antalet filialapotek som lyder under apoteken minskade under 2025. Detta påverkades åtminstone delvis av de besparingsåtgärder som förväntas riktas till apoteksverksamheten. För att säkerställa tillgången till apotekstjänster ändrade Fimea några av de minsta självständiga apoteken till filialapotek i situationer där det inte längre fanns verksamhetsförutsättningar för ett självständigt apotek. Fimea inrättade också enskilda nya apotek och omdefinierade gränserna för apotekens lokaliseringsområden så att apotekstjänster finns tillgängliga just där de behövs.
Anpassningar i språkkraven för förpackningspåskrifter gjordes för att förbättra tillgången
Läkemedelslagstiftningen förutsätter att nationella språk används för förpackningspåskrifterna. Från och med mars 2025 har läkemedelsföretagen kunnat ansöka om samnordiska läkemedelsförpackningar för sjukhuspreparat med engelskspråkiga texter via projektet Regulatory flexibility for common Nordic packages. Även på nordiska förpackningar för sjukhuspreparat är det primära alternativet de nationella språken, men om nationella språk krävs på kritiska läkemedel med liten efterfrågan är de möjligt att preparaten inte kan tillhandahållas.
I slutet av året underlättades tryggandet av tillgången genom att utöver engelska även tillåta andra EU-språk på förpackningarna vid behov. Genom denna förändring kunde man avsevärt utvidga möjligheterna att få tillgång till vissa sjukhuspreparat med mycket liten efterfrågan i Finland.
I och med projektet godkändes under 2025 engelskspråkiga förpackningar för 21 sjukhuspreparat.
Fimea tryggade tillgången till veterinärmedicinska läkemedel i störningssituationer
Störningar i tillgången till veterinärmedicinska läkemedel är ett globalt problem som framhävs på ett litet marknadsområde som Finland. Fimea fortsatte 2025 att vidta åtgärder för att förebygga störningar i tillgången och granskade bland annat möjligheterna att på ett kontrollerat sätt avvika från förpackningarnas språkkrav.
År 2025 förekom betydande och långvariga störningar i tillgången till exempelvis följande veterinärmedicinska läkemedel:
- Formalin som används i fiskodling och vars tillgänglighet förhindrades eftersom det veterinärmedicinska läkemedlet inte kunde fås till Finland och de övriga alternativen inte var lämpliga för näringen. Situationen behandlades i samarbete mellan flera myndigheter och sektorer, och fiskodlingsverksamheten tryggades slutligen genom en tillfällig lösning. På längre sikt är målet att även Finland ska få ett veterinärmedicinskt läkemedel med försäljningstillstånd.
- Kaliumbromid avsedd för hundar, vars störning i tillgången var EU-omfattande och gällde de enda två veterinärmedicinska läkemedlen med försäljningstillstånd i EU. Som ersättande preparat användes ex tempore -preparat samt veterinärmedicinska läkemedel med specialtillstånd från utanför EU.
- Influensa- och stelkrampsvaccin som är avsedda för hästar (de två mest använda i Finland) och vars störning i tillgången pågick nästan hela 2025. Störningarna kunde avhjälpas med andra motsvarande preparat med försäljningstillstånd.
-
Utbytet av biologiska läkemedel som inleddes i april 2024 utvidgades två gånger under 2025 och samtidigt förberedde man sig på den sista ibruktagningsfasen i början av 2026.
Läkare har sedan 2017 haft skyldigheten att förskriva det förmånligaste biologiska läkemedel som lämpar sig för behandling av patienten. Ibruktagandet av läkemedelsutbyte av biologiska läkemedel har gjort det möjligt att byta ut läkemedlet mot ett förmånligare preparat även på apotek.
Utbytet av biologiska läkemedel på apotek inleddes i april 2024 när de enoxaparinpreparat som används för att förebygga och behandla ventromboser blev de första biologiska läkemedlen som omfattades av utbytet av läkemedel på apotek. I januari 2025 blev det möjligt att byta ut alla andra biologiska läkemedel, med undantag för insulinpreparat, som används för att behandla till exempel reumatism, psoriasis, astma och inflammatoriska tarmsjukdomar.
Utbytet av läkemedel utvidgades i två omgångar till insulin som används vid behandling av diabetes. Utbytet av glargininsuliner inleddes 1.4.2025. Utbytet av andra långverkande insuliner utvidgades i början av 2026. Kortverkande insulin omfattas inte av läkemedelsutbytet och biologiska läkemedel för patienter under 18 år byts inte ut på apoteket.
Ur Säkerhets- och utvecklingscentret för läkemedelsområdet Fimeas synvinkel har ibruktagandet av utbytet av biologiska läkemedel framskridit enligt planen och på ett kontrollerat sätt.
Läkemedelsutbytet av biologiska läkemedel har medfört besparingar
Genom utbyte av biologiska läkemedel har man velat öka priskonkurrensen och minska kostnaderna för läkemedelsersättningar. Enligt de uppgifter som FPA publicerat verkar åtgärderna som främjar priskonkurrensen för biologiska läkemedel ha fungerat och sänkt ersättningskostnaderna avsevärt. Enligt de förhandsbedömningar som FPA publicerade i december 2025 kommer utgifterna för läkemedelsersättningar för de biologiska läkemedel för vilka det finns en biosimilar att vara cirka 41 miljoner euro mindre 2025 än 2022. FPA:s granskning från december gällde januari–september 2025, då alla andra biologiska läkemedel förutom insuliner har omfattats av utbytet. Granskningen under perioden april–september 2025 gällde också glargininsuliner som kom att omfattas av utbytet i april.
Genom rådgivning om hur dosdispensern ska användas säkerställs ett säkert utbyte av läkemedel
Ett biologiskt läkemedel är ett preparat vars aktiva substans är en biologisk substans. Ett biologiskt läkemedel ges i allmänhet genom infusion i en ven eller subkutan injektion. Recept på biologiska läkemedel är endast giltiga ett år åt gången.
En biosimilar är lika effektiv och lika säker som det ursprungliga biologiska läkemedlet. Den innehåller samma aktiva substans som det ursprungliga läkemedlet. Fimea fastställer sinsemellan utbytbara biologiska läkemedel fyra gånger per år. Med hjälp av Fimeas läkemedelsöktjänst kan man kontrollera vilka läkemedel som är biologiska läkemedel.
Det kan finnas skillnader i hur det ursprungliga biologiska läkemedlets respektive biosimilarens dosdispenser fungerar. För utbytbara preparat är dock dosdispensrarna så pass likadana att bytet kan göras säkert efter att apotekets farmaceutiska personal har gett produktrådgivning.
Fimea publicerade under ibruktagningsfasen i juli en söktjänst som sammanställer produktskillnaderna mellan biologiska läkemedel som stöd för apotekens läkemedelsrådgivning. Söktjänsten omfattar endast de mest centrala uppgifterna om läkemedelspreparat och deras produktskillnader. I söktjänsten har alla de inhalationsläkemedel och biologiska läkemedel sammanställts, för vilka Fimea har producerat tilläggsuppgifter om läkemedelsutbyte.
Läs mer
Läkemedelssöktjänst (Fimea.fi)
FPA:s forskningsblogg: Priskonkurrensen för biologiska läkemedel sparar tiotals miljoner (på finska)