Coronavaccinernas inrapporterade biverkningar
Fimea publicerar uppgifter om coronavaccinernas inrapporterade biverkningar på sin webbplats. En mer omfattande rapport publiceras på finska.
Viktig information för dem som anmäler biverkningar av coronavacciner
- Fimea ger inte medicinsk rådgivning till enskilda patienter. Farhågor och frågor om den egna vaccinationen ska utredas tillsammans med den egna vårdinstansen eller den vaccinerande enheten.
- Fimea ger ingen särskild bekräftelse på att det tagit emot en biverkningsanmälan och kommenterar inte heller anmälan om det inte finns behov av att be om ytterligare utredningar.
- Vanliga kända biverkningar av coronavaccinerna är feber, frossbrytningar, huvudvärk, trötthet, muskel- och ledvärk, förstorade och ömma lymfkörtlar, allergiska reaktioner, illamående, kräkningar, diarré och reaktioner i vaccinationsstället. Det är inte nödvändigt att anmäla dessa biverkningar.
Om biverkningsanmälningen gäller ett coronavaccin är det viktigt att rapportera vaccinets namn, samt om det är fråga om ett variantvaccin (t.ex. Comirnaty Original/Omicron BA.1, Comirnaty Original/Omicron BA.4-5 eller Spikevax bivalent Original/Omicron BA.1). Vaccinationsuppgifterna finns på webbtjänsten Mina Kanta-sidor.
- Avsikten med anmälningarna om biverkningar är att upptäcka nya och oväntade biverkningar. Med anmälningarna kartläggs inte biverkningarnas frekvens. Denna kan utredas genom undersökningar och via hälso- och sjukvårdsregistren.
- Vaccinbiverkningar och läkemedelsskador som berättigar till ersättning är inte alltid samma sak. Information om ersättning för skador orsakade av coronavacciner finns på Läkemedelsskadeförsäkringens webbplats.
- THL ansvarar för de vacciner som är i användning, för vaccinationsordningen och för de riksomfattande rekommendationerna som gäller riskgrupper. Kommunerna ansvarar för hur vaccinationerna ordnas. Mer information finns på den egna kommunens webbplats.
Ytterligare information: Att göra en biverkningsanmälan (Fimea)
Coronavaccinernas inrapporterade biverkningar i Fimeas register över biverkningar
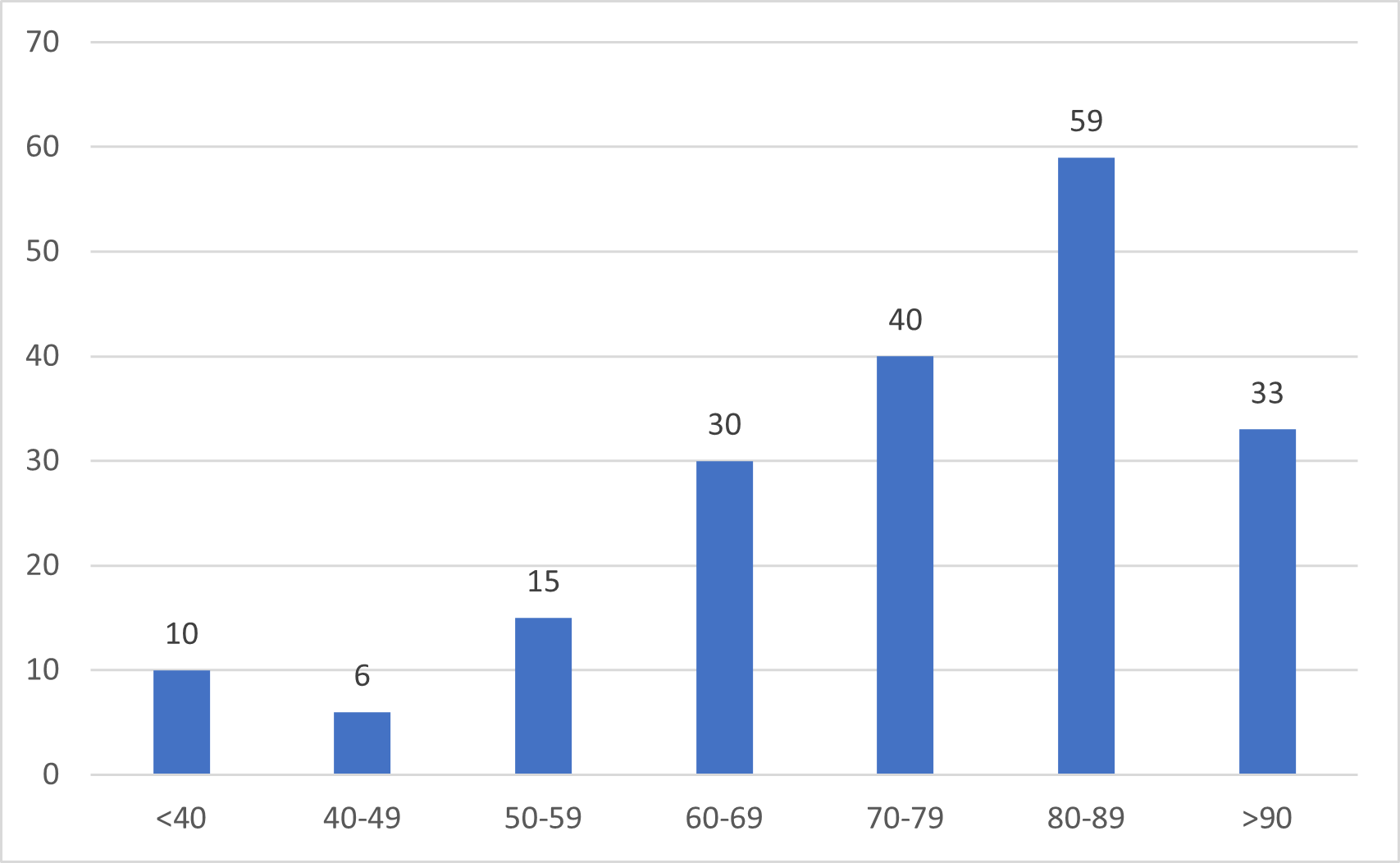
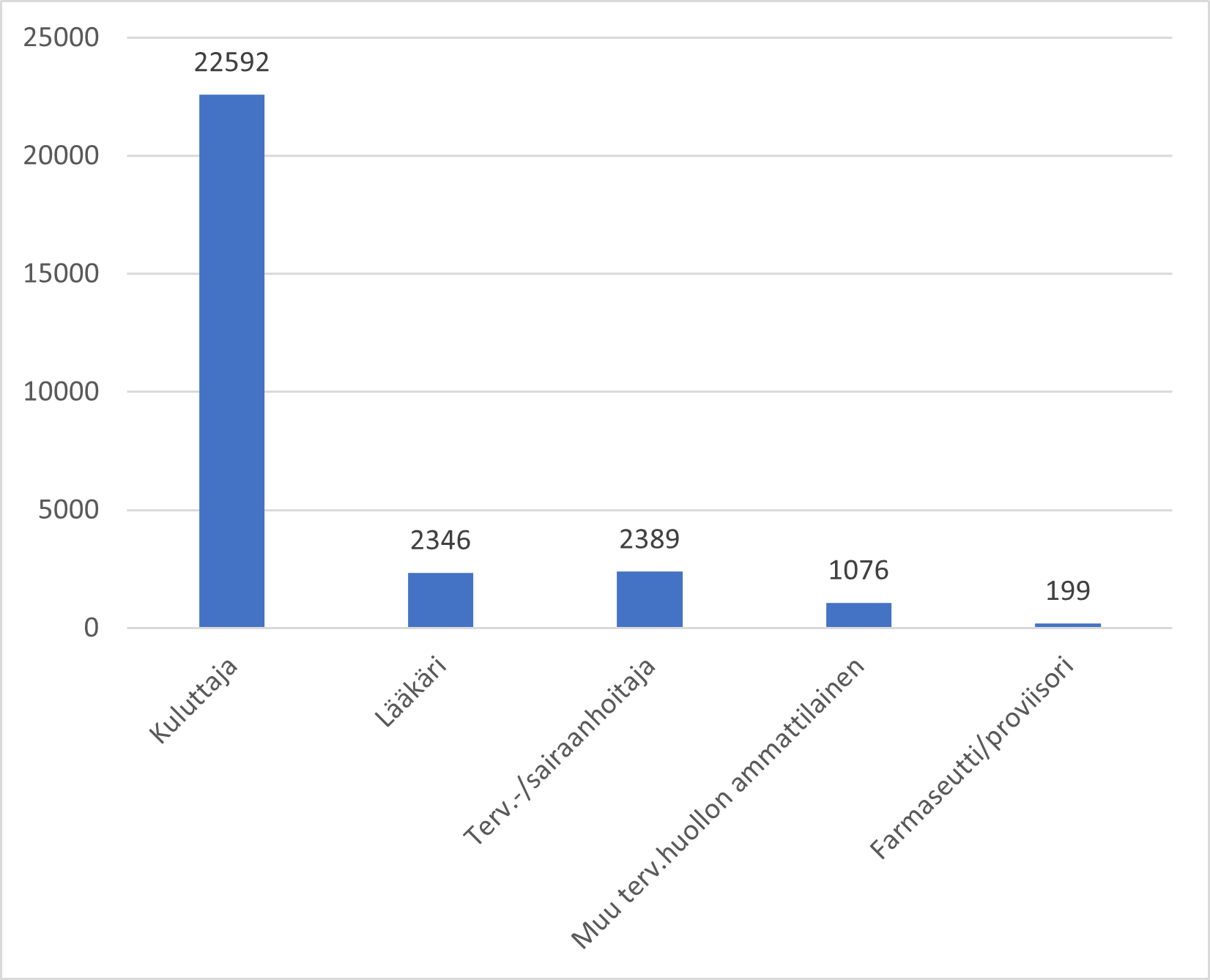
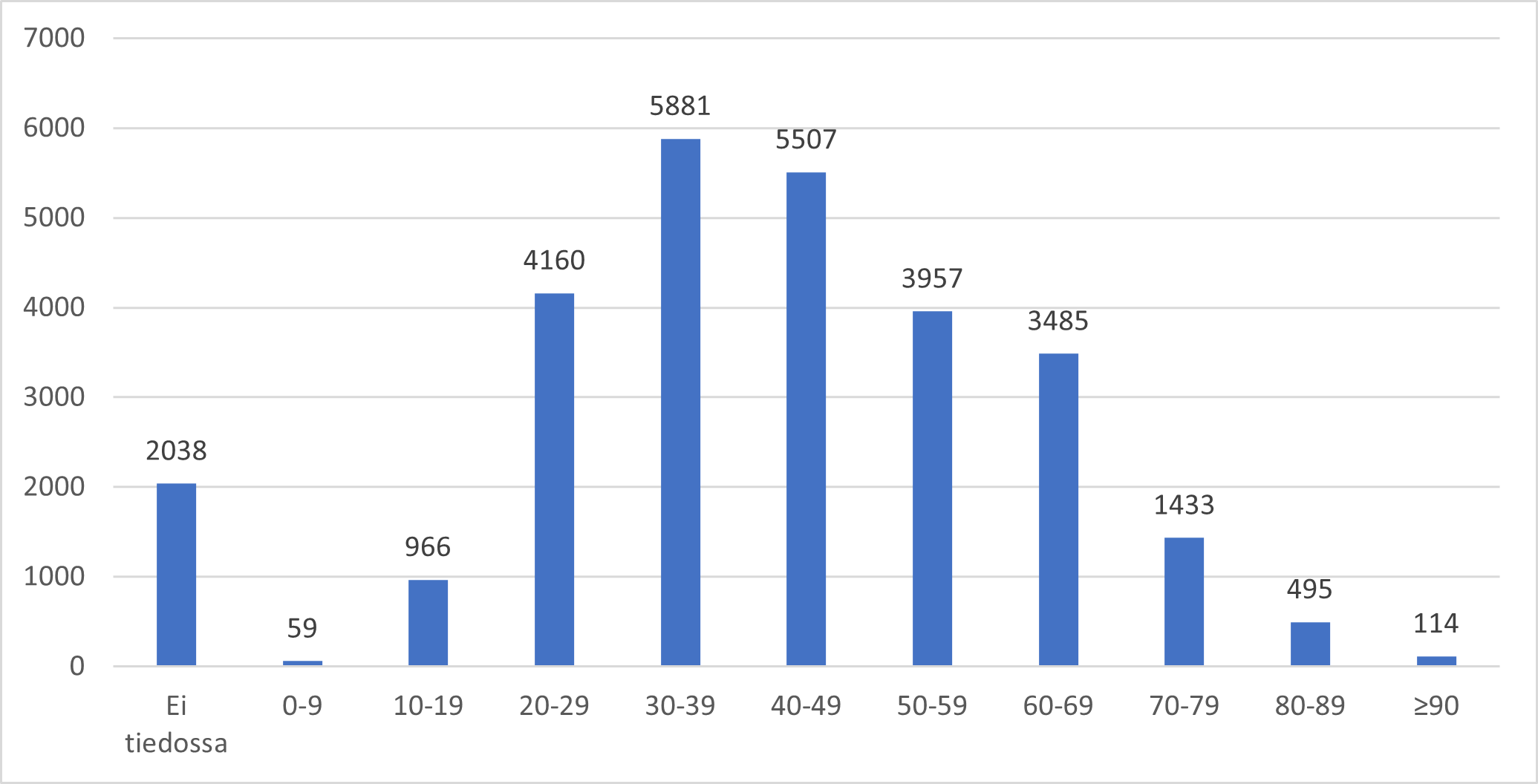
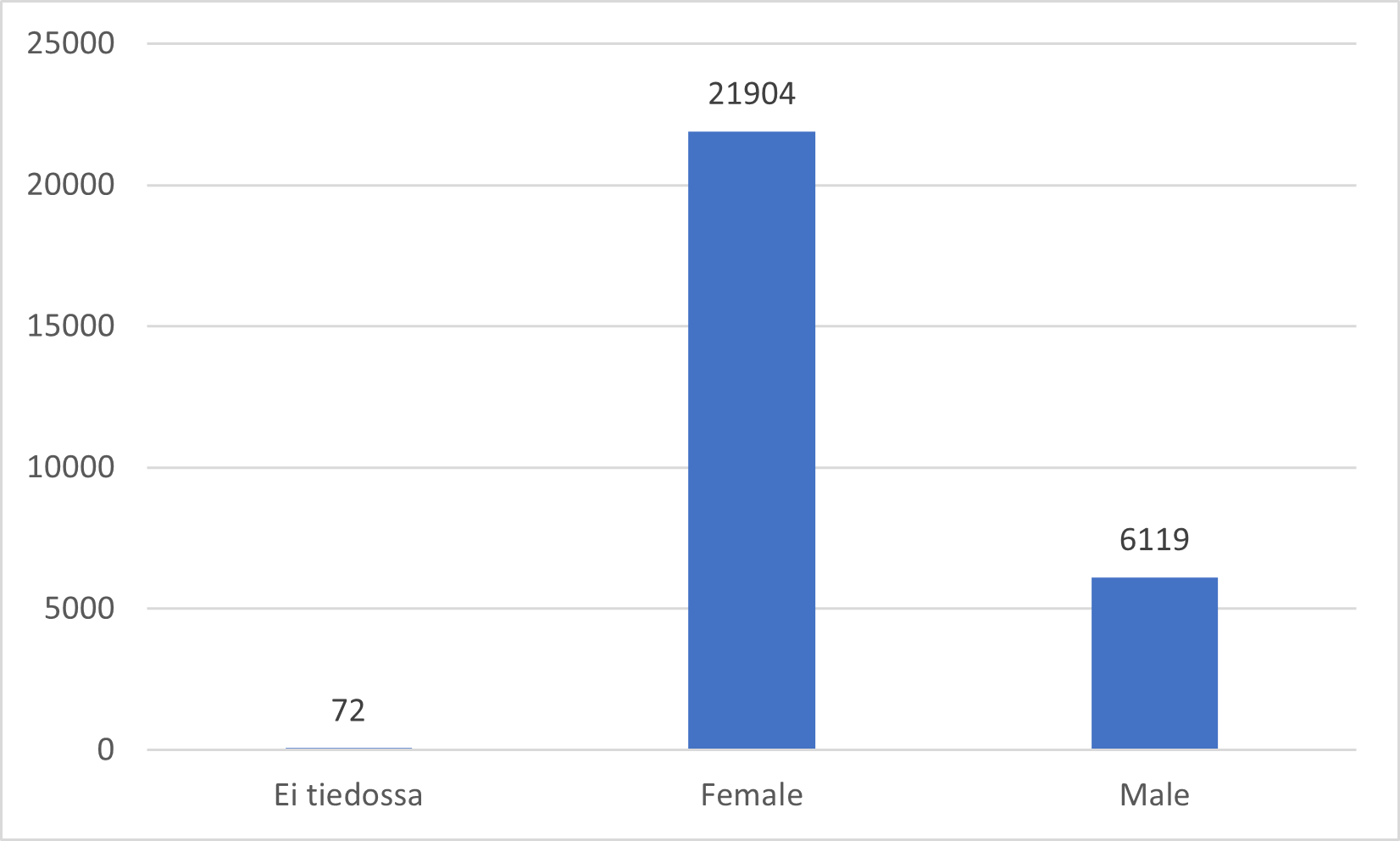
Antalet behandlade anmälningar 7.3.2024
| Vaccintyp (produktnamn) | Totalt antal anmälningar** | Icke-allvarliga anmälningar** | Allvarliga anmälningar*,** |
|---|---|---|---|
| mRNA-vaccin Comirnaty (inklusive variantvaccin) | 19809 | 14825 | 4984 |
| mRNA-vaccin Spikevax (Moderna) | 5675 | 4571 | 1104 |
| Adenovirusvektorvaccin Vaxzevria (AstraZeneca) | 2937 | 2060 | 913 |
| Adenovirusvektorvaccin Jcovden (COVID-19 Vaccine Janssen) | 14 | 9 | 5 |
| Proteinvaccin Nuvaxovid (Novavax) | 27 | 18 | 9 |
| Sammanlagt | 28498 | 21483 | 7015 |
* Bedömningen grundar sig på anmälarens bedömning, eller om den inte har meddelats, på Fimeas bedömning. En biverkning bedöms vara allvarlig om den har lett till död, livsfara, sjukhusvård eller förlängt den, orsakat en bestående skada, funktionsnedsättning eller är en medfödd missbildning.
** Det totala antalet kan vara mindre än summan av olika vacciner, eftersom det kan finnas flera misstänkta vacciner i anmälningarna.
Behandlingskön för coronavaccinernas biverkningsanmälningar, som formades under 2021, är avklarad och det finns inga anmälningar som väntar på behandling. Alla anmälningar som Fimea får behandlas utan dröjsmål.
Allvarlighetsbedömningen påverkar i första hand det hur brådskande anmälningarna behandlas och hur snabbt informationsutbytet sker mellan Fimea, Europeiska läkemedelsmyndighetens EudraVigilance-databas och innehavaren av försäljningstillståndet för vaccinet. Biverkningsanmälningar och eventuella signaler som följer av dem prioriteras och bedöms på medicinska grunder, inte enbart på basis av hur allvarlig anmälningen är.
I Finland används coronavacciner av olika tillverkare i olika mängd. För de vacciner som ges mest kommer också flest anmälningar. Baserat på antalet biverkningsanmälningar kan vaccinernas säkerhet inte jämföras sinsemellan. Information om hur vaccinationerna framskrider finns på THLs webbplats: Uppföljning av COVID-19 vaccinationerna.
Biverkningsanmälningarna beskriver anmälarens iakttagelser och uppfattningar, och betyder inte att ett eventuellt samband mellan vaccinet och de observerade verkningarna har bekräftats. Slutsatser om vaccinets nyttor och risker kan dras först när alla tillgängliga uppgifter har genomgått en vetenskaplig bedömning som är en del av vaccinets kontinuerliga säkerhetsuppföljning. Om ett säkerhetsproblem bekräftas, vidtas åtgärder för att uppdatera t.ex. produktinformationen och vaccinationsanvisningarna.
Rapporterade biverkningar
De anmälda biverkningarna av coronavaccin har listats separat för varje vaccin.
I de vaccinspecifika filerna granskas vaccinets alla biverkningar och allvarliga biverkningar med hjälp av diagram och tabeller. I tabellerna presenteras de vanligaste biverkningarna per organgrupp.
En anmälan innehåller i genomsnitt fem misstänkta biverkningar, och därför är antalet anmälda biverkningar större än antalet anmälningar. I en anmälan kan beskrivas att till exempel nässelutslag, illamående och huvudvärk, alltså tre olika biverkningar, uppkommit efter vaccinationen.
Bakgrundsinformation om biverkningsanmälningarna
Biverkningar: Skadliga och oavsedda effekter orsakade av ett läkemedel (30 a § i Läkemedelslagen)